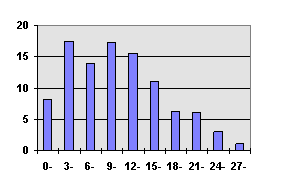
Forholdet mellom carotisstenose og anamnese
hos pasienter henvist for TIA ved karfysiologisk laboratorium
ved Institutt for fysiologi og biomedisinsk teknikk ved NTNU i
perioden 1990-1996
(ikke endelig versjon)
Hovedoppgave 1998
ved
Institutt for fysiologi og biomedisinsk teknikk
Av: stud. med. Rune Aakvik
Veileder: Stig Slørdahl
INNHOLD
Forord
Material og Metode
Resultater
Diskusjon
Konklusjon
Referanser
Vedlegg
RESULTAT- TABELLER OG DIAGRAMMER
REGISTRERINGSSKJEMA
HOVEDOPPGAVE STATISTIKKDATA
Tekniske apparater har alltid interessert meg. Det brakte meg til noen lærerike år på NTH før jeg startet på medisin. Første studieåret ble jeg tilbudt et studentprosjekt, "tumor volumberegning ved hjelp av tredimensjonal-ultralyd". Et spennende prosjekt hvor jeg kunne benytte tidligere tekniske fagkunnskaper knyttet opp mot en medisinsk vinklet forskningsoppgave. Jeg ønsket at ultralyd skille bli et tema i min oppgave. Ultralyd er en enkel, komplikasjonsfri og rimelig metode for å undersøke pasienter. Teknikken kan benyttes til å lage todimensjonale snittbilder, eller til å fremstille strømningshastigheter i blodkar. De første dopplersonografiapparatene kom til Norge i midten av 1970-årene, men ble først vanlige ut over i 1980-årene. Jeg fikk enkel opplæring i bruken av flere typer ultralydapparater, og studerte selv de tekniske prinsippene bak ultralyd. Deretter kom en fire måneders periode med opptak av målinger fra pasienter, men som ble brått avsluttet når noe av det teknisk utstyr forsvant og jeg kunne ikke fortsette. Dette ble en midlertidig slutt på ultralydeventyret. Det resulterte bare i noen få tredimensjonale fremstillinger som jeg senerer la ut på en Web-side på internett, og at jeg presenterte de midlertidig resultatene neste gang det ble utdelt studentprosjekter. Dette hadde vært lærerikt, og gitt meg en forsmak på det å skrive oppgave, og at det å samle inn data selv var meget tidkrevende. Etter noen år med slumring kom jeg på ny over en oppgave som benyttet seg av ultralyd. Karfysiologisk laboratorie, ved Institutt for fysiologi og biomedisinsk teknikk, brukte ultralyd til å undersøke carotisarteriene for stenoser ved hjelp av ekko-doppler-ultralyd. De hadde samlet ultralyddata og pasientanamneser i flere år, så her slapp jeg selv å gjøre undersøkelsene og det sparte meg for mye merarbeid med oppgaven. Denne oppgaven var godt egnet for meg hvor jeg fikk knytte sammen tekniske og medisinske kunnskaper.
Takk til veilederne mine Solveig Tingulstad og Sevald Berg, fra det første studentprosjektet, for å vekke i meg iveren etter å bruke tekniske nyvinninger for å hjelpe pasienter.
Takk til medisinsk biblotek for hjelpen med litterratursøkingen.
Takk til underviserne som ga gode tips om å skrive en hovedoppgave.
En spesiell takk for gode tips og godt samarbeide til min veileder Stig Slørdahl. Fagmessig kritikk og kommentarer på det jeg hadde gjort på oppgaven, fra diskusjoner med sistnevnte, inspirerte til nye vinkler å analysere problemene på, og hjelpen var oftest umiddelbar, og var viktig for progresjonene i oppgaven.
TRONDHEIM 1998
Rune Aakvik
Forholdet mellom carotisstenose og anamnese
Her presenteres et materiale på 365 pasienter, 152 kvinner, 213 menn, med henvisning til ultralyd halskar utredning, med diagnosen TIA (Transitorisk Ischemisk Attakk) som inklusjonskriterie, av disse hadde 63 carotisstenose. Disse dataene er hentet fra resultatene fra alle ultralyd halskar undersøkelser i årene1990-1996, fra undersøkelser ved Karfysiologisk laboratorium Institutt for fysiologi og biomedisinsk teknikk, NTNU.
Stenoser av halskar er en viktig årsak til iskemiske hjerneslag og den viktigste årsaken til TIA. Forsnevringer i halspulsåren gir iskemisk hjernesykdom ved at blodprobb (emboli) løsner fra veggpåleiringer. (arteriosklerotiske forandringer).
TIA er prognostisk for ny ateriosklerotisk vaskulær sykdom. Symptomene for TIA kan vi hente ut fra en standarisert anamnese, samt at mer generell arteriosklerotisk karsykdom kan hentes ut fra namnese om plager fra ben og brystet. Ankel-arm-indeks måling er en enkel test for å sjekke etter ateriosklerotisk vaskulær sykdom i underekstremitetene. Denne studien ser på hvordan diagnosen carotisstenose kan testes ved anamnese eller ved måling av ankel-arm-indeks, og sammenligning av disse to testenes diagnostiske kraft, i forhold til funnene ved ultralyd halskar. Anamnesen deles opp i tester for benplager, hjerteplager og hodeplager. Testen anamnese er positiv for 157 og finner 30 av carotisstenosene. Ankel-arm-indeks er positive for 69 av de har 31 carotisstenose. Hodeplager er positive for 208 og 36 av de har carotisstenose. Benplager er positive for 147 og 35 av de har carotisstenose. Henvisende diagnose TIA var 365 og 63 av disse hadde carotisstenose. Forholdene mellom disse tallene gir at ankel-arm-indeks er mere presis enn de andre testene til å detektere carotisstenose.
Stud. med. Rune Aakvik
Veileder Stig Slørdahl
This study reports of 365 patients, 152 women and 213 men, all referred for TIA were included in in this study. Mean age 62 years.
They were examined with doppler-ultrasound in the period 1990-1996, in the vascular fysiological laboratory of the Institute for fysiology and biomedical tecnics. Among these 63 had carotisstenosis (CS) diagnosed by doppler-ultrasound. A standarised anamnese of symptoms from the head, chest and legs were summarised, and beyond a given limit (12) were assigned to be tested anamnese positive. 157 were anamnese positive of these 30 had been diagnosed with carotisstenosis. The ankle-arm-index was measured and values lower than 0.9 were assigned to be testet ankle-arm-index positive. 69 were ankle-arm-index positive, of these 31 had been diagnosed with carotisstenosis.
31 CS out of 69 ankel-arm-index positive. 36 CS out of 208 headsymptoms positive. 35 CS out of 147 legsymptoms positive. 63 CS out of 365 TIA referred. These tests sensitivity, specificity and accuracy was calculated and compared, and ankle-arm-index had greater sensitivity, specificity and accuracy than the others. The conclusion is that measuring ankle-arm-index is a better way than getting the anamnese to predikt carotisstenosis. Testing with head symptoms, or referring diagnosis TIA, compared with the ankle-arm-index gave the same result.
Introduksjon
Hjerneslag er plutselig innsettende tap av kroppsfunksjon som er forårsaket av forstyrrelse i hjernens blodsirkulasjon. Det plutselige tapet av kroppsfunksjon spenner fra små og ubetydelige nevrologiske utfall som for eksempel lett nedsatt kraft i en ekstemitet, til omfattende og sammensatte funksjonstap av nær sagt alle kroppens funksjoner som styres av hjernen. Dersom de nevrologiske utfall varer mindre enn 24 timer bruker man betegnelsen TIA (transitorisk iskemisk attakk). Langt de fleste TIA varer mindre enn 1 time, som regel bare i minutter.
Slag kan skyldes utilstrekkelig blodforsyning til en del av hjernen på grunn av blodpropp som tilstopper et blodkar (hjerneinfarkt). Slike blodpropper kan oppstå på stedet (trombe), eller de fraktes med blodet fra hjertet eller precerebrale pulsårer (emboli). Infarkt er årsak til 85% av hjerneslagene. Veggpåleiringer (arteriosklerotiske forandringer) i de større pulsårer i hodet, på halsen eller i hovedpulsåren er den viktigste årsaken til TIA. Det er også vist at pasienter som har hatt iskemiske slag eller TIA fra fremre kretsløp og hvor det påvises innsnevring av halspulsåren (carotisstenose) på samme side, har en særlig høy risiko for nye slag. Ca 10% sannsynlighet for nytt slag pr år. [1] Denne risikoen kan reduseres betydelig ved kirurgisk inngrep på innsnevringen (enarterektomi) dersom diameterreduksjonen av karet er minst 70%. Denne gevinsten er betydelig. NASCET studien [2] viste at man sparte 17 slag ved å operere 100 pasienter. Det er derfor viktig å identifisere disse pasientene. Denne studien sammenligner flere metoder for å identifisere disse pasientene.
Referansemetoden, eller gullstandarden, for å klassifisere innsnevring i halspulsåren er å se på diameterreduksjonen av karet ved angiografi. Allikevel er rutinemetoden for å vurdere innsnevringer i halspulsåren ultralyd. Med ultralyd kan man visualisere veggpåleiringer, mens man med Doppler ultralyd kan måle blodstrømshastigheter og dermed gradere innsnevringer ved hjelp av hastighetsøkningen. En veggpåleiring som halverer arealet av blodkarets tverrsnitt vil gi en dobbling av blodstrømmens hastighet. Ultralyd er derfor en god metode for å utelukke innsnevringer i halspulsårene.
Det er allment akseptert at pasienter som har hatt et TIA anfall bør få undersøkt halspulsårene med ultralyd for å utelukke signifikante innsnvringer. Det er videre kjent at veggpåleiringer i et karområde øker muligheten for tilsvarende endringer andre plasser i kartreet. Hva en lege oppfatter som et sannsynlig TIA anfall kan nok variere ut fra kunnskap og erfaring hos den enkelte og også ut fra hvor mye tid som brukes på anamnesen. Ved Karfysiologisk laboratorium, Institutt for fysiologi og biomedisinsk teknikk, NTNU blir det brukt en standardisert anamnese i den hensikt å plukke ut symptomer på generell karsykdom.
Hensikten med denne studien har vært å se på sammenhengen mellom henvisningsdiagnosen TIA sammenholdt med et standard anamneseskjema og de funn som er gjort ved en ultralydundersøkelse av halskarene. Videre har jeg ønsket å se på sammenhengen mellom funn ved ultralydundersøkelse av halskar hos disse pasientene og målte ankel-arm-indekser, som gir et uttrykk for arteriell blodsirkulasjon i underekstremitetene.
For å kunne studere disse forholdene her har jeg gått igjennom alle pasientjournalene til pasienter som har vært henvist til Karfysiologisk laboratorium, Institutt for fysiologi og biomedisinsk teknikk, NTNU for mistenkt TIA i årene 1990-1996, hvor det samtidig er er gjort rutinemessige målinger av ankel-arm-indekser. Alle pasientene har også fylt ut et standard anamneseskjema (se vedlegg) som siden ble gjennomgått med sykepleier.
Undersøkelsen omfatter 365 pasienter, 152 kvinner og 213 menn. Gjennomsnittsalder var 62 år med 12 år som standardavvik. Alle pasienter i vår undersøkelse var henvist til ultralyd halskar med diagnosen TIA (Transitorisk Iskjemisk Attakk) ved Karfysiologisk laboratorium, Institutt for fysiologi og biomedisinsk teknikk, NTNU i perioden 1990-1996.
TIA er definert som fokalnevroligiske utfall som forsvinner i løpet av 24 timer. TIA skyldes oftest embolisering av blodplater/fibrin fra arteriosklerotiske lesjoner på arteria carotis/vertebralis, hovedpulsåren eller fra hjertet. Symptomene ved TIA kommer av plutselig tap av funksjon av en region av hjernen, og når ofte toppen på få minutter og varer i minutter til timer. De vanligste symptomer ved TIA er disse: Amaurosis fugax (kortvarig synstap, og er ofte første kliniske tegn på carotisstenose [3]), afasi (tapt taleevne), hemiparese (halvsidig lammelse), hemisensorisk følelsesutfall,(ikke smerte, berøring) synsfelt utfall er symptomer med forbigående okklusjon av fremre sirkulasjon, som har tilførsel fra carotis. Blodstrøm gjennom arteria vertebralis, forsyner den bakre sirkulasjon til hjernen. Ved affeksjon av denne er de vanligste symptomene: Diplopi (dobbeltsyn), vertigo (svimmelhet), oppkast, dysartri, hemisensorisk tap, transient global amnesi eller bevissthetstap.
Differensialdiagnoser som må utelukkes er fokale epileptiske anfall (hvor rykninger er det typiske), og migrene. Hodepine, svimmel, øresus og besvimelse er ikke vanlige symptom ved TIA [3].
Pasienter som var henvist til ultralyd halskar med andre diagnoser enn TIA ble ikke studert nærmere i denne undersøkelsen. Pasienter med henvisningsdiagnoseen amaurosis fugax er heller ikke tatt med.
De fleste henvisninger var fra allmennpraksis, mens noen få var henvist fra Regionsyskehuset i Trondheim-
Materialet er fremkommet ved en retrospektiv gjennomgang av pasientjournaler for perioden 1990 til 1996. Dataene ble nedskrevet på et registreringsskjema, og overført til Excel regneark, hvor beregningene ble utført.
Ultralyd
Prinsippet for ultralydundersøkelse av carotis er tidligere beskrevet i Tidsskriftet for den Norske Lægeforening.[4,5] Metoden er enkel, komplikasjonsfri og rimelig for å undersøke sirkulasjonsforhold. Pasientene ble undersøkt med en VingMed ultralydmaskin, CFM 750, med en 7 MHz transduser.
Prinsippet bak ultralyd må forklares med fysikken som beskriver den.
Strømningsfysikk (fluiddynamikk) beskriver hvordan væsker oppfører ved forskjellige strømningsforhold, og disse kan brukes til å beskrive strømningsforhold i blodkar.
Mengden av blod som strømmer gjennom et blodkar er fast, og kan ikke komprimeres eller reduseres uten at blod fjernes. Væske inn er lik væske ut. Dette gir kontinuitetsligningen.
A1*V1=A2*V2
Stenosen vil gi en økt strømningshastighet.
Dette kan si noe om grad av stenose. Det vil si reduksjon i tverrsnittsareal ved å måle hastigheten før (V1) og i (V2) stenosen.
% innsnevring = 100*A2/A1 [%] = 100*V1/V2 [%]
Poisevilles ligning fra fluiddynamikken forteller at motstanden til blodets strømning vil være proporsjonalt med 1/r4. Slik at for selv små endringer i radius når radiusen er liten blir endringen i strømning stor.Ved uregelmessig høye hastigheter, som ved stenoser, kan hastigheten til blodet i et punkt få hurtig vekslende karakter, både i retning og størrelse,turbulens oppstår.
Blodstrømmens hastighet varierer i pulser med tiden etter hjertets kontraksjon. Vi ser på topphastigheten som et uttrykk for gjennomsnittshastigheten i en laminær væskestrøm.
Prinsippet bak ultralydmåling av hastigheten til blod er basert på Doppler-effekten, som oppstår når en lydkilde er i bevegelse i forhold til mottager. Dette fenomenet kjenner vi igjen til daglig når en bil passerer oss. Det er en høyere frekvent lyd når den nærmer seg, og en lavere når den fjerner seg, enn frekvensen til lydkilden om den sto i ro. Frekvensforskjellen kan måles og hastigheten kan beregnes ut fra den og retningen.
Ultralyd kan brukes til å lage todimensjonale snittbilder med ekkoprinsippet. Et lydsignal sendes ut og når det treffer en flateovergang reflekteres en del av signalet, et ekko. Avstanden kan da regnes ut ved å måle tiden signalet bruker på å returnere, når lydhastigheten i vevet er kjent. For de fleste vev med mye væskeinnhold er hastigheten tilnærmet 1500 m/s mens den er en god del saktere for fett, som dermed vil gi forvrengning av bildet. Bein stopper lydsignalet, og et svart felt vil vises bak, likeledes for luftholdige tomrom (Tarm). Lydhastigheten er med på å bestemme hvor mange bilder som kan lages per sekund, vanlig rate er ca 30 bilder pr sekund. Styrken på ekkoet kodes om til intensiteten (brightness), derav navnet B-mode, og dette brukes til bilededannelsen. Når dette gjøres i en sektor, eller langs en linje, et lineært array, kan det brukes til å danne todimensjonale snitt bilder. Dette kan gi oss et bilde av det stenoserte halskaret som en innsnevring av lumen.
Grad av stenose blir vurdert og klassifisert ut i fra systolisk maksimalhastighet. Hastighetene ble delt inn i fire områder: normalområdet fra 0,3 til1,3 m/s, og moderat økt hastighet fra 1,3 til 1,8 m/s og høygradig stenose ved hastigheter over1,8 m/s, og redusert i området mindre enn 0,3 m/s, sistnevnte som tegn på totalokklusjon. Disse ble da klassifisert med tallverdi [0-3], etter økende grad av stenose, fra normalt til stenose og videre i til sannsynlig totalokklusjon. Denne inndelingen er valgt ut fra klinsk praksis, men flere andre studier har benyttet seg av den samme [6], eller lignende inndeling for å klassifisere stenoser. Grad av stenose kan også graderes ut i fra det todimensjonale bildet,ved å se på diameter til blodkaret målt i B-Mode på ultralydapparatet, hvor man får et snittbilde av arterien og kan måle den interne diameteren direkte, og derav detektere en stenose.
Det ble også registrert om funn av plaque og turbulens i carotis, men hverken disse eller diagnosen "intern/ekstern"-stenose, (om stenosen var i carotis interna eller externa) var medbestemmende for diagnosen carotisstenose som ble definert. Carotisstenose ble definert diagnostisert for verdier utenom normalområdet av strømningshastigheter for carotis interna eller carotis communis, økte strømningshastigheter eller patologisk lave, det vil si klassifiseringsverdi over 0, altså [1-3]. Som igjen vil si hastigheter mindre enn 0,3 m/s eller over 1,3 m/s. Kun carotis interna ble registrert for det er den gir blodstrøm til den fremre sirkulasjonen av hjernen, og stenose i denne eller embolier fra den kan gi iskemi. Carotis externa gir blodstrøm til overfladiske ansikts og hodestrukturer.
Ankel-arm-indeks
Ankel-arm-indeks (AAI), er et ikke invasivt hemodynamisk billig mål på perifer arteriell karsykdom, og finnes ved å måle systolisk blodtrykk i ankel og arm og dele disse på hverandre. Trykkmålinger er den viktigste ikke invasive test for nedsatt arteriell sirkulasjon i underekstremitetene. Hvis trykket i ankelen er større eller lik trykket i overekstremiteten, er sannsynligheten for en stenose i underekstremiteten liten. Trykket måles ved at man plasserer en vanlig blodtrykksmansjett omkring ankelen og blåser opp til suprasystolisk trykk. For å registrere blodstrømmen i arterien brukes et Doppler apparat. Da kan bare det systoliske blodtrykket som måles. Indeksen som kommer frem ved å dele systolisk ankel blodtrykk på arm systolisk blodtrykk kalles Ankel-arm-indeks (AAI).
Flere studier [7,8,9,10] viser at et lavt AAI har en høy prediktiv verdi for tilstedeværelse av arteriell atherosclerotisk okkluderende karsykdom, og påfølgende økt kardiovaskulær sykelighet og dødelighet.
AAI vil variere etter hvilke blodkar som legges til grunn for målingene. Det kan være sideforskjell i blodtrykket på høyre og venstre arm. I leggen eller på foten er det tre blodkar som kan brukes til å måle blodtrykket på leggen, de to vanligste å bruke er a. tibialis posterior (TP) og a. dorsalis pedis (DP). [7] viser at AAI for TP er 0,04 høyere enn for DP i gjennomsnitt. Alle blodtrykk måles på både venstre og høyre side for blodkarene a. brachialis, a. tibialis posterior og a. dorsalis pedis. Disse målingene gjentas tre ganger, og ut i fra disse verdiene utregnes det en gjennomsnitts AAI.
Usikkerheten om nedre normalområde for AAI, gjør at grenseverdien for patologisk AAI varierer noe mellom forskjellige studier, fra 0,8-0,98 i [10,11,12,13]. Variasjon av verdien til grenseverdien for patologisk AAI vil påvirke estimatet av prevalensen av perifer arteriell karsykdom i stor grad. Grenseverdien 0,9 for patologisk lav AAI, er valgt på bakgrunn av at dette er en hyppig brukt verdi i andre studier [10,14, 15]. Klinisk gjenspeiler dette seg med at AAI testen gir egnede verdier på sensitivitet og spesifisitet som gjør den godt egnet til en screening test.
AAI måles for blodtrykk i hvile. Andre studier viser at AAI ved fysisk aktivitet kan gi patologisk utslag, mens det kan være normalt i hvile på grunn av tilstrekkelig kollateral blodstrøm rundt den arterielle stenosen. [7]
Sprørreskjemaet
Spørreskjemaet, her referert til som Anamnesen, var delt inn i tre hoveddeler som hver tok for seg plager fra henholdsvis hjertet (brystet), bena og hodet. [Se vedlagt spørreskjema.]
Alle pasientene som ble henvist måtte svare på et spørreskjema, med spørsmål
om røyking, medikamentbruk, symptomer og plager fra hjertet, bena og hodet.
I spørreskjemaet er det videre registrert kjønn, alder, røykerstatus, tidligere sykdommer, og nåværende medisinbruk, men i undersøkelsen her ble kun alder og kjønn brukt til å klassifiere populasjonen i undergrupper, for så å se om det er forskjeller mellom disse undergruppene.
Spørsmålene om hjerteplager går på smerter/ubehag/trykk/tyngdefornemmelse i brystet, og om disse oppstår/lindres/vedvarer ved visse aktiviteter. Disse plagene summeres som antall "Ja" på svarskjemaet. Antallet hjerteplager ligger i området [0-8]. Alle spørsmålene skal da trekke i retning av iskemise symptom. Her er intensjonen at et "ja" kan være uttrykk for iskemisk hjertesykdom .
Benplager registrerer om pasienten har smerter i bena ved gange/hvile, om de lindres av hvile eller lindres av videre aktivitet. Antall "ja" gir antallet benplager som ligger i området [0-9], og kan være et uttrykk for iskemisk sykdom i bein.
Hodeplager registrerer synsutfall, dobbeltsyn, lammelse/ svekkelse/ følelsesløshet/ prikking i kroppen svimmelhet, vertigo. Antall "ja" gir antallet hodeplager som ligger i området [0-14]. Disse symptomene skal ha karakter av lokal nedsatt funksjon i hjernen på iskemisk grunnlag.
Disse plagene vi ønsker å få frem har symptomer som har sin årsak i iskjemi, på grunn av utilstrekkelig blodtilførsel. Alvorligheten av symptomene den nedsatte blodforsyning reflekterer, gjenspeilerer grad av stenose, eller sagt på en annen måte som grad av generell ateriosklerose, etter hvert som embolier og tromber stenger igjen karene.
Summen av disse plagene, summen av hjerteplager, hodeplage og benplager, gir en anamnestisk tallverdi 0 til 31. Dette er en praktisk, men ikke statistisk korrekt måte å slå sammen resultatene fra hjerteplager, hodeplage og benplager. Dersom denne summen overstiger en viss grenseverdi, her valgt til 12 eller større, defineres pasienten til å være positiv for anamnesen, og blir gitt verdien 1, mens pasienten er negativ for anamnesen, og får verdien 0 om den anamnestisk tallverdi er mindre enn den valgte grenseverdi. Tilsvarende er det valgt grenser for hjerteplager, benplager og hodeplager. For alle disse er 5 valgt som grense. Disse grensene er valgt tilfeldig, og er valgt ut i fra kliniske praktiske forhold. Økes grensen blir resultet mer spesifikt på bekostning av en mindre sensistivitet. Her er det ikke diskutert om det er statistisk korrekt eller ei å summere disse plagene, det gjøres senere.
Definisjon av statistikkbegreper
Sensitivitet, spesifisitet, positiv prediktiv verdi, negativ prediktiv verdi, likelihood ratio og nøyaktighet regnes ut for hver enkelt diagnostisk test. Disse størrelsene er definert på følgende måte. [20,21,22]
Sykdom
|
Test |
Ja |
Nei |
|
|
Ja |
a |
b |
a+b, positivt testet |
|
Nei |
c |
d |
c+d, negativt testet |
|
|
a+c, syke |
b+d, friske |
a+b+c+d, populasjonen i testen |
Sensitivitet = a/(a+c), andel av de syke som er testet positivt.
Spesifisitet = d/(b+d), andel av de friske testet negativt.
Positiv prediktiv verdi = a/(a+b), sannsynlighet for å ha sykdom når testet positiv.
Negativ prediktiv verdi = d/(c+d), sannsynlighet for ikke å ha sykdom når testet negativ.
Likelihood ratio = (a/(a+c)) /(b/(b+d))
Nøyaktighet = (a+d)/(a+b+c+d), andel av testresultater som er korrekte.
Valg av grenseverdier:
Valg av grenseverdier for at anamnesen eller ankel-arm-indeks skal være positiv eller negativ, er bestemmende for disse undersøkelsesmetodenes sensitivitet, spesifisitet, positiv prediktiv verdi, negativ prediktiv verdi, likelihood ratio og nøyaktighet.
En grenseverdi som gir for høy sensitivitet vil i tillegg til de sanne pasientene fange opp mange friske og diagnostisere disse som syke, og noe slikt kan resultere i overundersøkelse eller overbehandling eventuelt feilbehandling av pasienter. En grenseverdi som gir for lav sensitivitet vil ikke fange opp tilstrekkelig av de syke pasientene, og de mister den hjelp de har krav på, men færre friske får diagnosen syk. Grenseverdien må bestemmes på grunnlag av klinisk skjønn, og nøyaktigheten den gir til testen, og hvilken praktisk nytte den kan tilføre hverdagen i klinikken.
Tabell #
|
Anamnesegrense |
10 |
11 |
12 |
13 |
14 |
15 |
|
|
Antall |
203 |
184 |
157 |
137 |
118 |
100 |
|
|
Sensitivitet |
0,62 |
0,54 |
0,48 |
0,41 |
0,38 |
0,30 |
|
|
Spesifisitet |
0,46 |
0,50 |
0,58 |
0,63 |
0,69 |
0,73 |
|
|
Positiv prediktiv verdi |
0,19 |
0,18 |
0,19 |
0,19 |
0,20 |
0,19 |
|
|
Negativ prediktiv verdi |
0,85 |
0,84 |
0,84 |
0,84 |
0,84 |
0,83 |
|
|
Nøyaktighet |
0,48 |
0,51 |
0,56 |
0,59 |
0,64 |
0,66 |
|
|
Likelihood ratio |
1,14 |
1,09 |
1,13 |
1,12 |
1,22 |
1,12 |
|
Tabell#
|
Hodegrense |
4 |
5 |
6 |
7 |
8 |
|
|
Antall |
261 |
208 |
148 |
110 |
72 |
|
|
Sensitivitet |
0,65 |
0,57 |
0,37 |
0,30 |
0,17 |
|
|
Spesifisitet |
0,27 |
0,43 |
0,59 |
0,70 |
0,80 |
|
|
Positiv prediktiv verdi |
0,16 |
0,17 |
0,16 |
0,17 |
0,15 |
|
|
Negativ prediktiv verdi |
0,79 |
0,83 |
0,82 |
0,83 |
0,82 |
|
|
Nøyaktighet |
0,34 |
0,45 |
0,55 |
0,63 |
0,69 |
|
|
Likelihood ratio |
0,89 |
1,00 |
0,88 |
1,00 |
0,86 |
|
Tabell #
|
Bengrense |
4 |
5 |
6 |
7 |
|
|
Antall |
161 |
147 |
126 |
77 |
|
|
Sensitivitet |
0,59 |
0,56 |
0,51 |
0,35 |
|
|
Spesifisitet |
0,59 |
0,63 |
0,69 |
0,82 |
|
|
Positiv prediktiv verdi |
0,23 |
0,24 |
0,25 |
0,29 |
|
|
Negativ prediktiv verdi |
0,87 |
0,87 |
0,87 |
0,86 |
|
|
Nøyaktighet |
0,59 |
0,62 |
0,66 |
0,74 |
|
|
Likelihood ratio |
1,43 |
1,50 |
1,63 |
1,92 |
|
Tabell #
|
Ankel-arm-indeksgrense |
0,80 |
0,85 |
0,90 |
0,95 |
1,00 |
|
|
Antall |
50 |
57 |
69 |
99 |
135 |
|
|
Sensitivitet |
0,38 |
0,43 |
0,49 |
0,62 |
0,73 |
|
|
Spesifisitet |
0,91 |
0,90 |
0,87 |
0,80 |
0,71 |
|
|
Positiv prediktiv verdi |
0,48 |
0,47 |
0,45 |
0,39 |
0,34 |
|
|
Negativ prediktiv verdi |
0,88 |
0,88 |
0,89 |
0,91 |
0,93 |
|
|
Nøyaktighet |
0,82 |
0,82 |
0,81 |
0,77 |
0,71 |
|
|
Likelihood ratio |
4,42 |
4,31 |
3,91 |
3,12 |
2,48 |
|
63 av 365 (17%) av pasienten henvist til ultralyd halskar med diagnosen TIA og hvor der forelå rutinemessig målt ankel-arm-indekser, fikk påvist stenose i a. carotis communis eller a. carotis interna.
Grenseverdier
Her ble grenseverdiene for testene satt til bestemte verdier på skjønnsmessig grunnlag.
5 eller større i anamnese-testene for hodeplager, hjerteplager og benplager.
Carotisstenose gitt ved hodeplager hadde da sensitivitet 0,57, spesifisitet 0,43, positiv prediktiv verdi 0,17, negativ prediktiv verdi 0,83, nøyaktighet 0,45, likelihoodratio 1.
208 (57 %) av 365 pasienter hadde da positiv anamnese for hodeplager.
Carotisstenose gitt ved benplager hadde da sensitivitet 0,56, spesifisitet 0,63, positiv prediktiv verdi 0,24, negativ prediktiv verdi 0,87, nøyaktighet 0,62, likelihoodratio 1,5. 147 (40%) av 365 pasienter hadde da positiv anamnese for benplager.
12 eller større som grense på anamnese-testen, med summen av hjerte, ben og hodeplager. Carotisstenose gitt ved anamnese hadde da sensitivitet 0,48, spesifisitet 0,58, postitiv prediktiv verdi 0,19, negativ prediktiv verdi 0,84, nøyaktighet 0,56, likelihoodratio 1,13.157 (43%) av 365 pasienter hadde da positiv anamnese.
Mindre enn 0.90 som grensverdi på ankel-arm-indeksen. [14,16,17,18] forteller om at også de undersøkelsene bruker <0,90 som grense, og den er god til å brukes som test i å finne sannsynlighet for arteriosklerostisk sykdom. Carotisstenose gitt ved ankel-arm-indeksen hadde da sensitivitet 0,49, spesifisitet 0,87, postitiv prediktiv verdi 0,45, negativ prediktiv verdi 0,89, nøyaktighet 0,81, likelihoodratio 3,91.
69 (19%) av 365 pasienter hadde AAI under grenseverdien 0,90.
Sammenheng anamnese og ultralydfunn.
Ut fra de valgte grenseverdier hadde 36 de 208 pasientene med positiv anamnese for hodeplager en carotisstenose. Tilsvarende hadde 35 av 147 med positiv anamnese for benplager en carotisstenose, mens hvis anamnesen ble sett under ette med grenseverdi 12 hadde 30 av 157 pasienter en carotisstenose.
Tabell #
|
Frekvensfordeling av anamnese |
||||||||||
|
365 |
0- |
3- |
6- |
9- |
12- |
15- |
18- |
21- |
24- |
27- |
|
n |
30 |
64 |
51 |
63 |
57 |
40 |
23 |
22 |
11 |
4 |
Gjennomsnittsverdi 10,8, median 11, standardavvik 6,5.
Diagram # :Frekvensdiagram for anamnese.

Av frekvensdiagrammet og tabellen for anamnesen ser vi at den har en topp rundt 9-12, mens hovedtyngden befinner seg nedfor anamnesegrensen som er 12, 208 pasienter som utgjør 57 %, mens 157 eller 43 % er testet anamnese positive. Kun 1 av pasientene med carotisstenose har ingen "ja" svar i anamnesen.
Sammenheng ankel-arm-indeks og ultralydfunn.
69 av de 365 pasientene som inngår i materialet hadde patologiske ankel-arm-indekser (<0,9) som uttrykk for nedsatt arteriell sirkulasjon.
Av de pasientene som hadde patologiske ankel-arm-indekser, hadde nesten halvparten (44,9%) påvisbare carotisstenoser nemlig 31 av 69 pasienter.
Tabell #
|
Frekvens av ankel-arm-indeks |
|||||||||||
|
365 |
0,3- |
0,4- |
0,5- |
0,6- |
0,7- |
0,8- |
0,9- |
1,0- |
1,1- |
1,2- |
1,3- |
|
n |
3 |
6 |
12 |
12 |
17 |
19 |
56 |
102 |
102 |
29 |
7 |
Gjennomsnittsverdi 1,01, median 1,06 standardavvik 0,19.
Diagram # :Frekvensdiagram over ankel-arm-indeks.
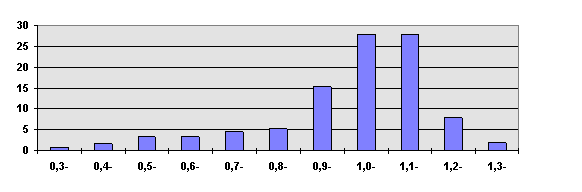 Frekvensdiagrammet over ankel-arm-indeks viser en tilnærmet normalfordeling, med topp i området 1,0-1,1. Dette området inneholder en stor andel av verdiene, ca 56 % av målingene befinner seg der. Andelen av de som har carotisstenose øker med synkende verdi av ankel-arm-indeks, fra ca 20% ved AAI 1.0 til 75 % ved 0,5. Slik at det absolutte antall pasienter med carotisstenose er omtrentlig likt i hvert 0,1 intervall i intervallet [0,4-1,1] for AAI.
Frekvensdiagrammet over ankel-arm-indeks viser en tilnærmet normalfordeling, med topp i området 1,0-1,1. Dette området inneholder en stor andel av verdiene, ca 56 % av målingene befinner seg der. Andelen av de som har carotisstenose øker med synkende verdi av ankel-arm-indeks, fra ca 20% ved AAI 1.0 til 75 % ved 0,5. Slik at det absolutte antall pasienter med carotisstenose er omtrentlig likt i hvert 0,1 intervall i intervallet [0,4-1,1] for AAI.
Sammenheng ankel-arm-indeks og benplager.
(Antall med carotisstenose ført opp i parentes.)
|
Ankel-arm-indeks |
Sensitivitet |
0,7 |
|||||||||||
|
+ |
- |
Spesifisitet |
0,67 |
||||||||||
|
Benplager |
+ |
48 |
99 |
147 |
Positiv prediktiv verdi |
0,33 |
|||||||
|
- |
21 |
197 |
218 |
Negativ prediktiv verdi |
0,9 |
||||||||
|
69 |
296 |
365 |
Nøyaktighet |
0,67 |
|||||||||
|
Likelihood ratio |
2,08 |
||||||||||||
48 av de 69 pasienten med patologe ankel-arm-indekser hadde en positiv anamnese fro benplager. Dette gir en sensitivitet på 0,7, spesifisitet 0,67 for å finne patologiske ankel-arm-indekser hvis pasienten angir en positiv anamnese på benplager.
Sammenheng ankel-arm-indeks og hodeplager.
(Antall med carotisstenose ført opp i parentes.)
|
Ankel-arm-indeks |
Sensitivitet |
0,55 |
|||||||||||
|
+ |
- |
Spesifisitet |
0,43 |
||||||||||
|
Hodplager |
+ |
38 (17) |
170(19) |
208 |
Positiv prediktiv verdi |
0,18 |
|||||||
|
- |
31 |
126 |
157 |
Negativ prediktiv verdi |
0,8 |
||||||||
|
69 |
296 |
365 |
Nøyaktighet |
0,45 |
|||||||||
|
Likelihood ratio |
0,96 |
||||||||||||
38 (55%) av pasientene med patologiske ankel-arm-indekser, hadde også positiv anamnese for hodeplager. Dette var ikke overraskende siden alle pasientene var henvist for TIA, men det viser at en kombinasjon med positiv anamnese for hodeplager og patologisk ankel-arm-indeks er langt mer sikker indikator for å plukke ut sannsynlig påvisbar carotisstenose ved ultralyd enn anamnese alene.
Sammenheng ankel-arm-indeks og anamnese.
(Antall med carotisstenose ført opp i parentes.)
|
Ankel-arm-indeks |
Sensitivitet |
0,64 |
|||||||||||
|
+ |
- |
Spesifisitet |
0,62 |
||||||||||
|
|
+ |
44 |
113 |
157 |
Positiv prediktiv verdi |
0,28 |
|||||||
|
- |
25 |
183 |
208 |
Negativ prediktiv verdi |
0,88 |
||||||||
|
69 |
296 |
365 |
Nøyaktighet |
0,62 |
|||||||||
|
Likelihood ratio |
1,67 |
||||||||||||
44 (64%) av pasienten med patologisk ankel-arm-indeks hadde også en positiv anamnese vurdert ut fra hele anamnesesystemet. Det gir en sensitivitet på 0,64 og spesifistet på 0,62 for å finne positiv ankel-arm-indeks når anamnesen er positiv.
Kombinasjon av ankel-arm-indeks og hodeplager.
38 av pasienten var både ankel-arm-indeks patologe og hadde hodeplager, og av disse hadde 17 carotisstenose.
|
Carotisstenose |
Sensitivitet |
0,27 |
|||||||||||
|
+ |
- |
Spesifisitet |
0,93 |
||||||||||
|
Hodep & AAI |
+ |
17 |
21 |
38 |
Positiv prediktiv verdi |
0,45 |
|||||||
|
- |
46 |
281 |
327 |
Negativ prediktiv verdi |
0,86 |
||||||||
|
63 |
302 |
365 |
Nøyaktighet |
0,82 |
|||||||||
|
Likelihood ratio |
3,88 |
||||||||||||
Kombinasjonen av å bade ha positiv anamnese for hodeplager og patologisk ankel-arm-indeks ga sensitivitet 0,27, spesifisitet 0,93, positiv prediktiv verdi 0,45, negativ prediktiv verdi 0,86, nøyaktighet 0,82, likelihood ratio 3,88.
Den høye spesifisteten gir at samfall av å bade ha positiv anamnese for hodeplager og patologisk ankel-arm-indeks gir meget stor sannsynlighet for å ha carotisstenose.
Kombinasjon av ankel-arm-indeks og anamnese.
20 av 44 ankel-arm-indeks patologe og anamnesepositive med carotisstenose.
|
Carotisstenose |
Sensitivitet |
0,32 |
|||||||||||
|
+ |
- |
Spesifisitet |
0,92 |
||||||||||
|
Anamn & AAI |
+ |
20 |
24 |
44 |
Positiv prediktiv verdi |
0,45 |
|||||||
|
- |
43 |
278 |
321 |
Negativ prediktiv verdi |
0,87 |
||||||||
|
63 |
302 |
365 |
Nøyaktighet |
0,82 |
|||||||||
|
Likelihood ratio |
3,99 |
||||||||||||
Kombinasjonen av å bade ha positiv anamnese og patologisk ankel-arm-indeks ga sensitivitet 0,32, spesifisitet 0,92, positiv prediktiv verdi 0,45, negativ prediktiv verdi 0,87, nøyaktighet 0,82, likelihood ratio 3,99.
Den høye spesifisteten gir at samfall av å bade ha positiv anamnese og patologisk ankel-arm-indeks gir meget stor sannsynlighet for å ha carotisstenose.
Diagram #
Aldersfordeling i populasjonen, inndelt etter kjønn og carotisstenose.
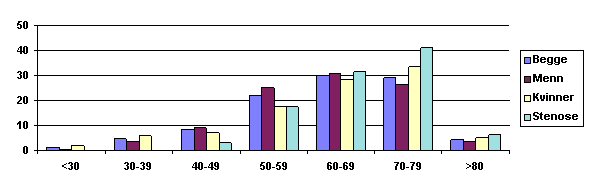 Vedrørende alder har populasjonen av menn og kvinner lik gjennomsnittsalder på 62-63 år, mens den er noe eldre for populasjonen som har carotisstenose der den er ca 69 år, og at de fleste med carotisstenose ligger i aldersgruppen 60-80 år. Det vil si at alder har stor prognostisk betydning for sannsynligheten for å ha en carotisstenose.
Vedrørende alder har populasjonen av menn og kvinner lik gjennomsnittsalder på 62-63 år, mens den er noe eldre for populasjonen som har carotisstenose der den er ca 69 år, og at de fleste med carotisstenose ligger i aldersgruppen 60-80 år. Det vil si at alder har stor prognostisk betydning for sannsynligheten for å ha en carotisstenose.
Tabellen viser at det er en opphopning av pasienter rundt aldersgruppen 60-69 år, både hos menn, kvinner og de med carotisstenose.
Diagram #
Frekvensdiagram av pasienter med carotisstenose.
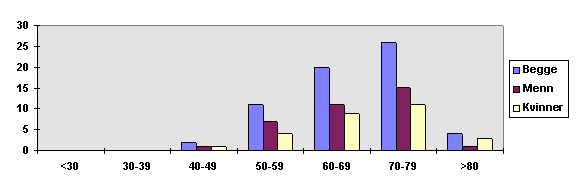 Grafen viser at jevnt over er carotisstenose hyppigere hos menn enn kvinner i alle aldersklasser bortsett fra de over 80 år.
Grafen viser at jevnt over er carotisstenose hyppigere hos menn enn kvinner i alle aldersklasser bortsett fra de over 80 år.
Ankel-arm-indeks og alder
Diagram #
Scatterplot av alder og ankel-arm-indeks.
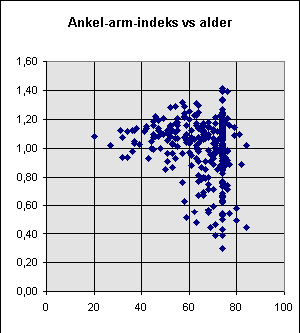
Ankel-arm-indeks plottet opp mot alder viser at ankel-arm-indeksen faller med økende alder, utregnet med lineær regresjon for vårt materiale faller den ca. 0,27/100 år. Grafen viser også at det er en del tilfeller med økt ankel-arm-indeks, det vil si verdier over 1,3 til 1,4, dette på grunn av at blodkarene blir stive [14]. Dette kan komme av at det er vanskelig å øke trykket nok i blodtrykksmansjetten til å komprimere blodkaret, med resultatet i at en for høy verdi måles.
Normalverdien er satt til å ha verdier over 0,9.
De forskjellige testenes evne til å velge ut populasjonen av carotisstenose.
[Antall carotisstenose delt på den utvalgte populasjon som er diagnostisert positive]
|
Henvist for TIA |
63/365 |
= 17,3 |
% |
|
Hodeplager |
36/208 |
= 17,3 |
% |
|
Benplager |
35/147 |
= 23,8 |
% |
|
Anamnese |
30/157 |
= 19,1 |
% |
|
Ankel-arm-indeks |
31/69 |
= 44,9 |
% |
Ankel-arm-indeks har da en nøyaktighet i sin populasjon av positive testet på 44,9 %, som omtrent er det dobbelte av hva de andre testene har, henholdsvis hodeplager har en nøyaktighet på 17,3 %, benplager 23,8 %, anamnese 19,1 % og henvisende diagnose TIA 17,3 %.
Pasientpopulasjonen som blir undersøkt ved karfysiologisk laboratorium, Institutt for fysiologi og biomedisinsk teknikk, NTNU, er en heterogen gruppe på grunn av at kriteriene for å henvise til ultralyd undersøkelse er liberale. For å ensarte og begrense populasjonen ble de som hadde TIA som henvisende diagnose valgt ut. Amaurosis fugax er regnet under TIA men er her tatt ut siden de hadde egen henvisende diagnose, og at dette pasientmaterialet inneholder færre funn sammenlignet med de med TIA.
Undersøkelsen de utfører inneholder ikke bare selve ultralyd undersøkelsen, men også en standardisert anamnese av pasienten, og en undersøkelse av blodtrykk og ankel-arm-indeks. Dette ga et rikt materiale til å kunne utføre flere typer statistiske undersøkelser blant pasientgruppen. Noe som savnes her er auskultasjon av carotis etter stenoselyd.
Gitt at måling av ankel-arm-indeks er en sensitiv test for screening av perifer vaskulær sykdom, og at tilstedeværelsen av en slik faktor er en viktig risikofaktor for død på grunn av hjerteinfarkt, hjerneinfarkt eller lungeemboli, demonstreres det her at den er en kraftig prediktor for slik karsykdom.
Utstyret som brukes har avansert teknikk, slik at metoden med dopplerteknikk for å måle blodstrømshastigheter kan kombineres med todimensjonale ultralydbilder (B-mode), slik at arteriosklerotiske forandringer og stenoser lettere kan påvises.
Anamnese og blodtrykksmåling til beregning av ankel-arm-indeks er enkle og billige undersøkelser som lett kan utføres i allmennpraksis. Det vil derfor ville kunne være enkelt å bruke disse testene til å screene store befolkningsmasser for å finne risikoindivider for arteriosklerotisk sykdom, her sett på som carotisstenose, og kunne tilby tidlig diagnostikk, utredning og behandling til disse.
Metoden kan også brukes til å følge en utvikling over tid. Metoden med å mål blodtrykkene og regne ut ankel-arm-indeks har vært i bruk siden slutten av 1970-årene som en screening test for okkult perifer vaskulær sykdom. Denne kan predikere risiko for vaskulær sykdom som koronarsykdom, iskemisk cerorovaskulær sykdom og iskjemisk sykdom i bena, og skyldes nedsatt arteriell sirkulasjon. I spørreskjemaet er det videre registrert kjønn, alder, røykerstatus, tidligere sykdommer, og nåværende medisinbruk, men i undersøkelsen her ble kun alder og kjønn brukt til å klassifiere populasjonen i undergrupper, for så å se om det er forskjeller mellom disse undergruppene. [7,8,9,10] Tilstander som i alvorligste tilfeller kan føre til død.
I det standardiserte spørreskjemaet, som er basert på et skjema fra en amerikansk undersøkelse, og som for det meste bare en oversettelse til norsk., kunne det vært hensiktsmessig å detektere bedre flere risikofaktorer for arteriosklerotisk sykdom. Hypertensjon, diabetes mellitus, alder er tatt med på skjemaet, men familiær opphopning av hjerte/kar-sykdom, røyking, p-piller, alkoholforbruk er ikke med. Andre predisponerende tilstander for TIA er hjertesykdom i form av klaffesykdom og rytmeforstyrrelser (spesielt atrieflimmer).
For hvert antall av hodeplager, var andelen av de med carotisstenose, nokså konstant i hvert intervall (Ca 20%), sett bort fra ytterpunktene. [Ref. tabell # hodplager] Fordelingen var slik at de med 3-7 symptomer fra hodet utgjorde størstedelen av de med carotisstenose. Bare 3 stykker hadde ingen symptomer fra hodet, men hadde likevel bekreftet carotisstenose (3/63 = 5 %) ved ultralyd. Dette kan anvendes klinisk i det at ingen symptomer fra hodet nesten utelukker at det er carotisstenose, med den inverse % gir dette ca 95 % sannsynlighet for at en carotisstenose da er utelukket. Men vi må ha i bakhodet at disse tallene gjelder for en TIA populasjon, og ikke en normalpopulasjon som bare er et tilfeldig utsnitt av befolkningen.
Symptomer fra hodet forventes å øke i samsvar med den generelle arteriosklerose av halskar, som er med på å gi symptomene. Flere av spørsmålene fra anamnesen om hodeplager går direkte på symptomer på TIA, så ut i fra dette kan en si at sannsynligheten for å ha hatt et TIA er stort når pasienten er testet positiv på hodeplager. Tabellen viser at det er moderate verdier for sensibilitet, spesifisitet og nøyaktighet til testen hodeplager til å forutsi carotisstenose
Benplagene gir et uttrykk for den generelle ateriosklerosen i bena, og det samme vil ankel-arm-indeks gjøre, slik at det forventes et samsvar mellom de to størrelsene. Vi ser her at benplager er en god test til å forutsi om ankel-arm-indeks er testet positiv, det er relativt høye verdier for sensitivitet, spesifisitet og nøyaktighet.
Populasjonen vi har valgt ut var en TIA henvist gruppe, og ikke uventet gjenspeiler dette seg i at det er få pasienter som har få eller ingen plager fra hodet (11/365), mens det er forholdsvis mange som ikke har symptomer fra hjertet eller bena, 177 som har ingen symptomer i bena og 158 som ikke har symptomer fra hjertet. Hodeplagene er tilnærmet normalfordelt med en topp rundt 5. [Ref. tabeller og diagram over hodplager, benplager, hjerteplager]
Hodeplager registrerer synsutfall, dobbeltsyn, lammelse/ svekkelse/ følelsesløshet/ prikking i kroppen svimmelhet, vertigo. Antallet hodeplager ligger i området [0-14].
Symptomene som hodeplager registrerer er typiske symptomer for TIA, reversible nevrologiske utfall med en varighet mindre enn 24 timer. Når det settes 5 som grenseverdi for positiv anamnese på hodeplager har 208 av pasientene (57 %) blitt definert diagnostisert TIA positiv.
Bruken av anmnese som test som er en sum av testene for hodeplager, benplager og hjerteplager, er kommet frem som praktisk bruk av hele anamneseskjemaet for plager, og er med sitt valg av grenseverdi, en bedre prediktor enn testen for hodeplager for å diagnostisere carotisstenose. En skulle tro at en test som gikk direkte på symtomer som kunne ha sin årsak fra kompromittering av den fremre precerbrale blodforsyning, som hodeplager, ville være bedre, men dette var ikke tilfelle. Testene anmnese, hodeplager, benplager og hjerteplager, er ikke godt sammenlignbare. De har forskjellig antall spørsmål, de tre sistnevnte har henholdsvis 14, 9 og 8 spørmål. Samme antall spørsmål for alle testene, for eksempel tre spørsmål, valgt ut med omhu fra spørreskjemaet, kunne være en spesifikk nok test på å detektere iskemisymptomer i den søkte regionen. Spørreskjemaet var oversatt fra en amerikansk studie, og er blitt brukt i noe modifisert form ved Karfysiologisk laboratorium, Instittutt for fysiologi og biomedisinsk teknikk, NTNU, i fra slutten av 80 tallet frem til dags dato. Spørsmålene kunne jeg ikke ha endret, men jeg kunne ha valgt ut noen nøkkelspørsmål til hver symtomregion, men jeg valgte å ta med alle spørsmålene og bare summere antallet spørsmål med positivt utslag. Noen spørsmål måtte jeg omformulere slik at "ja" alltid ga utslag i retning av iskemisk symptomatologi.
Frekvensdiagram for pasienter med carotisstenose viser at jevnt over er carotisstenose hyppigere hos menn enn kvinner i aldersgruppen under 80 år. Dette kan ha å gjøre med den generelle trenden av at menn rammes på et tidligere tidspunkt av hjerte- karsykdom, mens kvinnene først tar igjen mennene flere år etter at de har passert menopausen, sammen med at kvinner har en gjennomsnittlig lengre levealder enn menn.
De forskjellige testenes evne til å velge ut populasjonen av carotisstenose.
44,9 % nøyaktighet ved Ankel-arm-indeks positiv testet.
17,3% nøyaktighet ved hodeplager positiv testet.
17,3% nøyaktighet ved Ankel-arm-indeks positiv testet.
Ankel-arm-indeks-testen er da over dobbelt så presis som både henvisende leges skjønn på å diagnostisere TIA til å detektere carotisstenose, og testen hodeplager.
Feilkilder:
Gjentatte målinger av strømningshastighet med doppler ultralyd av samme halskar fra en annen studie [6] viste standardavvik (SD) mindre enn 10 % av gjennomsnittet. En relativt god reproduserbarhet. Reproduserbarheten blir vanskeligere ved en svær stenose når hastigheten ofte varierer sterkt. Som tidligere nevnt vil selv en liten radiusendring da føre til store endringer i hastigheten til blodstrømmen.
En må anta at utstyret er feilfritt og ikke er en kilde til feil data, og at det i såfall genererer en systematisk feil, og at det heller ikke er legen som måler feil.
Ved totalokklusjon blir strømningshastigheten veldig liten eller faller bort, og det kan være vanskelig å vite om man måler i åren eller i en annen struktur når man vanskelig kan identifisere arterien sikkert. Dette kan føre til forveksling av carotis externa og interna ved målinger.
Ved måling av ankel-arm-indeks ble hver blodtrykkmåling gjentatt tre ganger og en gjennomsnittsverdi utregnet. Arteriosklerose i beina kan være så alvorlig at blodkarene ikke er kompressible, og vil gi blodtrykkverdier som blir feilmålt til alt for høye verdier. Disse pasientene er de som har alvorligst grad av arteriosklerose.
Spørsmål nr. 6 i anamnesen om benplager kan være tvetydig."Forsvinner plagene noen ganger når du går på flat mark. Claudicatio intermittens kan få dempet symptomatologi når personen har gått seg varm, dette på grunn av at oppvarmet muskulatur har større vasodilatasjon med dertil økt perfusjon av vevet og minsket symptomatologi til følge.
Her forsøker man å utelukke muskel/skjelett lidelser (bløtdelslidelser) ved at symptomene skal ha typisk iskemisk karakter. Tilstander som isjias, podagra, senebetennelser, leddskader, reumatisme eller andre bløtdelsskader som kan gi smerter i bena, skal ikke gi utslag på anamnesen av plager fra bena.
Tilstander som kan imitere TIA, slik som epilepsi, migrene og multippel sclerose, og kunne være kilde til ubegrunnet inkludering i studien.
I målingene fra de første årene datainnsamlingen ble utført, 1990-1991, ble ikke ankel-arm-indeks konsekvent målt når henvisende diagnose var TIA. I den perioden var det mest claudicatiohenvisninger som det ble målt ankel-arm-indeks på. Disse kasusene som manglet ankel-arm-indeks utgjorde ca 120 stk, mot ca 80 inkluderbare kasus fra denne perioden.
Av de ikke-inkluderte kasusene var det 12 som hadde carotisstenose, og de fleste av disse var anamnese positive, og hadde store utslag på benplager som tegn på generell arteriosklerose i bena, og det kan forventes et tilsvarende utslag i senkning av ankel-arm-indeks. Et såpass stort hull i materialet kan jo forskyve resultatet en del. Fra slutten av 1991 ble både anamnese og ankel-arm-indeks konsekvent tatt med i undersøkelsen, og materialet fra etter den tiden inneholder få kasus som ble ekskludert på grunn av mangelfull utfylling av skjema.
Anamnese som sum av hodeplager, benplager og hjerteplager kan ikke sies å være statistisk korrekt, men i klinisk sammenheng gir den en praktisk test, som er bedre enn for eksempel hodeplager, men den er dårligere enn testen med ankel-arm-indeks.
I denne studien viste det seg at ankel-arm-indeks hadde nøyaktigere diagnostisk verdi, og bedre sensitivitet og spesifisitet enn en standardisert anamnese ved testing for å diagnostisere carotisstenose. Dette svaret er overens med undersøkelsene i [14,16,17,18].
Ankel-arm-indeks var omlag dobbelt så presis til å predikere carotisstenose som testene for anamnese, hodeplager, benplager og henvisende diagnose TIA.
Når anamnesen angående symptomer fra hodet, hodeplager, ikke inneholder symptomer utelukker dette carotisstenose med ca 95 % sannsynlighet, og dermed kan anamnesen anvendes i en rask screening undersøkelse når carotisstenose mistenkes.
Referanser